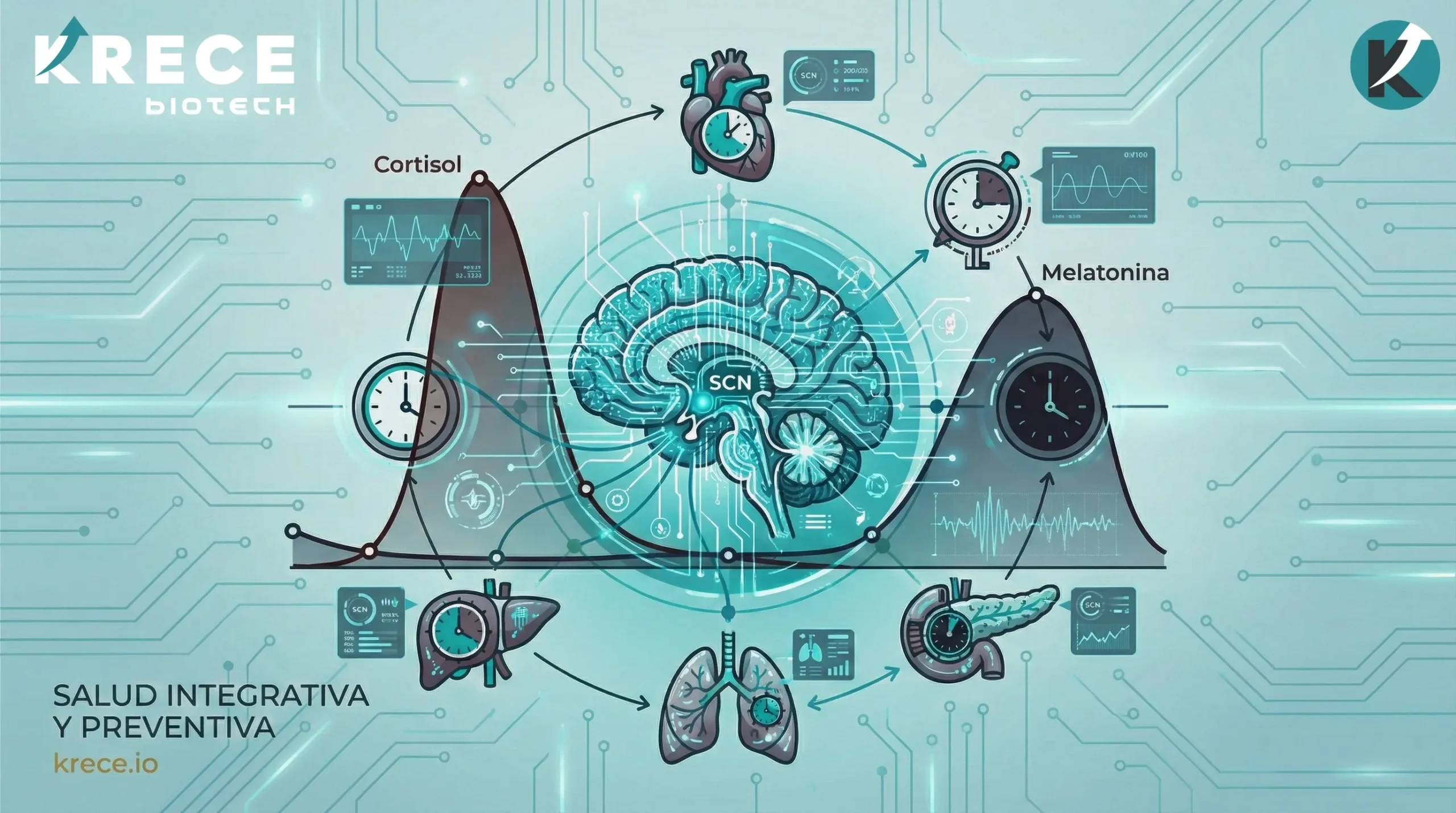
El ritmo circadiano y la secreción hormonal constituyen la arquitectura temporal que regula la homeostasis sistémica y la eficiencia de la señalización endocrina a lo largo del ciclo de 24 horas.
La homeostasis, lejos de ser un estado de equilibrio constante, es un proceso dinámico y predictivo en el que el organismo anticipa demandas metabólicas y ambientales. El sistema circadiano constituye el marco regulatorio que orquesta la secreción hormonal, asegurando que los procesos fisiológicos ocurran en el momento óptimo del ciclo de 24 horas.
El tiempo es, por tanto, una variable biológica fundamental. La eficiencia de la señalización hormonal —desde la sensibilidad a la insulina hasta la respuesta al estrés mediada por el eje HPA y la regulación sistémica del cortisol— depende de la integridad de este sistema interno de sincronización.
Ritmo circadiano: arquitectura jerárquica del sistema
El sistema circadiano en mamíferos se estructura de forma jerárquica, distinguiendo entre un marcapasos central y una red de relojes periféricos distribuidos en prácticamente todos los tejidos del organismo.
El núcleo supraquiasmático (SCN)
Situado en el hipotálamo anterior, el núcleo supraquiasmático actúa como el reloj maestro. Este centro integrador recibe información fótica directa a través del tracto retinohipotalámico y sincroniza los ritmos internos con el ciclo geofísico de luz–oscuridad.
A nivel molecular, esta oscilación se mantiene mediante bucles de retroalimentación transcripcional y traduccional que involucran genes reloj específicos (Clock, Bmal1, Per, Cry), cuya expresión rítmica determina la temporalidad de múltiples procesos celulares.
Relojes periféricos y desacoplamiento interno
Subordinados al SCN, los órganos periféricos —hígado, páncreas, tejido adiposo y músculo esquelético— poseen su propia maquinaria circadiana. Estos relojes locales regulan funciones específicas, como la homeostasis de la glucosa hepática o la lipólisis en el tejido adiposo.
Aunque el SCN sincroniza estos tejidos principalmente a través de señales humorales (glucocorticoides) y nerviosas (sistema nervioso autónomo), los relojes periféricos pueden desacoplarse del reloj central cuando reciben señales contradictorias, dando lugar a un estado de desincronización interna.
Ritmo circadiano y zeitgebers: señalización ambiental
La sincronización del sistema circadiano con el entorno depende de claves externas denominadas zeitgebers (dadores de tiempo).
- Luz: principal sincronizador del SCN. La exposición lumínica, especialmente en el espectro azul, suprime la secreción de melatonina y señala el inicio de la fase activa.
- Alimentación (crononutrición): sincronizador dominante de los relojes periféricos, en especial el hepático. La ingesta activa vías metabólicas como mTOR e insulina, capaces de modificar la fase circadiana periférica de forma independiente al ciclo luz–oscuridad.
- Actividad física y temperatura: actúan como señales de refuerzo que influyen en la expresión génica muscular y la función mitocondrial.
Ritmo circadiano y secreción hormonal
La secreción hormonal sigue patrones pulsátiles y circadianos diseñados para optimizar la fisiología durante las fases de actividad (día) y reposo (noche).
Eje cortisol–melatonina
Estas dos hormonas operan en contrafase y constituyen la señal endocrina primaria del ritmo día–noche.
- Cortisol: presenta un nadir nocturno y un incremento progresivo hacia la madrugada, culminando en el Cortisol Awakening Response (CAR). Este pico representa una señal anticipatoria de activación metabólica, no una respuesta al estrés agudo.
- Melatonina: sintetizada en condiciones de oscuridad, actúa como regulador sistémico del reposo, modulando temperatura corporal, presión arterial y función inmune.
Insulina y metabolismo de la glucosa
La tolerancia a la glucosa y la sensibilidad a la insulina muestran una clara variación diurna. La capacidad de respuesta de las células beta pancreáticas y de los tejidos diana es mayor en la mañana y disminuye progresivamente a lo largo del día.
La interacción entre melatonina e insulina es directa: el receptor MT2, expresado en las células beta, inhibe la secreción de insulina durante la noche biológica, explicando la respuesta glucémica exacerbada cuando la ingesta ocurre en fases de melatonina elevada.
Hormona del crecimiento (GH) y lipólisis
La secreción de GH es predominantemente nocturna y se asocia al sueño de ondas lentas. Además de su papel anabólico, promueve la lipólisis y la gluconeogénesis durante el ayuno nocturno, preservando glucosa para el sistema nervioso central.
Ritmo circadiano, secreción hormonal y cronodisrupción
La cronodisrupción surge cuando existe un desajuste crónico entre el sistema circadiano interno, los ritmos conductuales y los ciclos ambientales.
Aplanamiento de los ritmos hormonales
Una característica distintiva del envejecimiento y de la disfunción circadiana es la pérdida de amplitud rítmica. Se observa un perfil hormonal aplanado, con cortisol elevado por la noche y reducido por la mañana, o una secreción de melatonina atenuada. Este ruido endocrino impide a los tejidos distinguir claramente entre fases de reposo y actividad.
Resistencia a la insulina inducida por el tiempo
La desalineación circadiana —como ocurre en el trabajo por turnos o la ingesta nocturna— induce resistencia a la insulina fisiológica. Al forzar el procesamiento de sustratos energéticos en momentos de baja capacidad mitocondrial, se favorece la lipotoxicidad y la acumulación ectópica de grasa.
Inflamación sistémica y estrés oxidativo
La expresión circadiana regula la actividad inmunitaria. La pérdida de ritmicidad se asocia a una elevación basal de marcadores inflamatorios y a una reducción de la capacidad antioxidante nocturna, conectando la cronodisrupción con la inflamación crónica de bajo grado y los procesos de envejecimiento fisiológico.
Responsabilidad editorial
Este marco establece por qué el tiempo biológico actúa como variable transversal en la regulación hormonal, el metabolismo y la inflamación, sirviendo de base estructural para análisis posteriores sobre cronodisrupción, estrés crónico y resiliencia fisiológica dentro del ecosistema KRECE.
Este contenido forma parte del proyecto editorial KRECE, una plataforma independiente dedicada al análisis, síntesis y divulgación de evidencia científica en salud, longevidad y biología humana.
Los artículos publicados en KRECE se elaboran a partir de literatura científica revisada (revisiones sistemáticas, meta-análisis y ensayos clínicos), utilizando metodologías de evaluación estructurada como el marco PICO (Población, Intervención, Comparación y Resultados).
El contenido se elabora utilizando herramientas de apoyo para el análisis y síntesis de información, bajo un modelo de supervisión humana constante. La interpretación biológica, la validación de fuentes y la decisión final de publicación corresponden siempre al equipo editorial de KRECE.
Puedes conocer en detalle nuestra metodología y principios editoriales en:
📐 Ver esquema editorial KRECE
Cluster estructural del silo Hormonas. Define el tiempo biológico como variable endocrina transversal. Contenido dependiente de los cornerstones de cortisol y señalización energética. No clínico. No prescriptivo.
La integridad del sistema circadiano trasciende la regulación del ciclo sueño-vigilia; representa el eje temporal que coordina la función endocrina global. La capacidad del organismo para mantener la homeostasis depende estrictamente de la sincronización precisa entre el reloj central y los osciladores periféricos.
En este contexto, la cronodisrupción no debe interpretarse meramente como una alteración del descanso, sino como un fallo sistémico en la señalización celular. La pérdida de la arquitectura temporal —manifestada a través del aplanamiento de las curvas hormonales y la desincronización de los relojes tisulares— constituye un mecanismo fisiopatológico subyacente que precede y exacerba la disfunción metabólica, la inflamación crónica de bajo grado y el envejecimiento biológico acelerado.