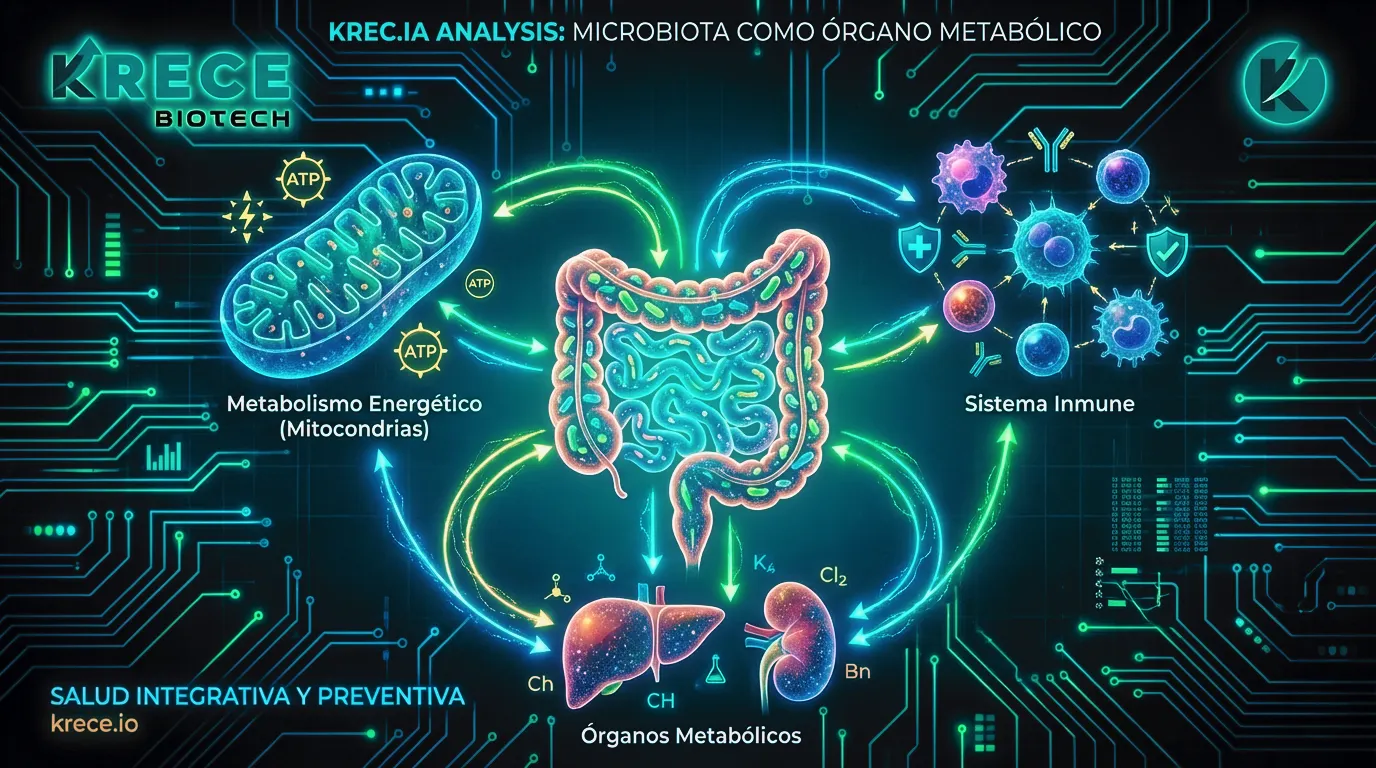
El envejecimiento biológico no es un proceso pasivo de deterioro cronológico, sino la consecuencia acumulativa de una desregulación en los sistemas de mantenimiento de la homeostasis. En el centro de esta pérdida de equilibrio se encuentra el concepto de inflammaging: un estado de inflamación crónica, estéril y de bajo grado que acelera la senescencia celular y tisular. Aunque históricamente se atribuyó este fenómeno exclusivamente a la inmunosenescencia intrínseca, la evidencia mecanística actual sitúa a la microbiota como órgano metabólico y de señalización en el eje causal de esta inflamación sistémica.
La microbiota intestinal no actúa simplemente como un ecosistema residente, sino como un modulador primario del tono inmunológico del huésped. La interacción entre los microorganismos luminales y el sistema inmune innato determina si el organismo opera en un estado de tolerancia fisiológica o bajo una alerta inflamatoria persistente.
Microbiota e inflamación basal
El sistema inmune de mucosas (GALT) alberga la mayor concentración de células inmunitarias del organismo y se encuentra en constante comunicación con el microbioma. En condiciones de eubiosis, esta interacción promueve un entorno antiinflamatorio, educando a las células T reguladoras (Treg) para mantener la tolerancia sistémica.
Sin embargo, las alteraciones en la composición y diversidad microbiana (disbiosis) modifican el perfil de señalización. La pérdida de especies comensales clave y la proliferación de patobiontes generan un entorno proinflamatorio local que, si se mantiene en el tiempo, trasciende el compartimento intestinal para convertirse en una señalización sistémica de estrés. Esta inflamación basal no responde a una infección aguda, sino a una carga antigénica constante que mantiene al sistema inmune en una activación subclínica permanente.
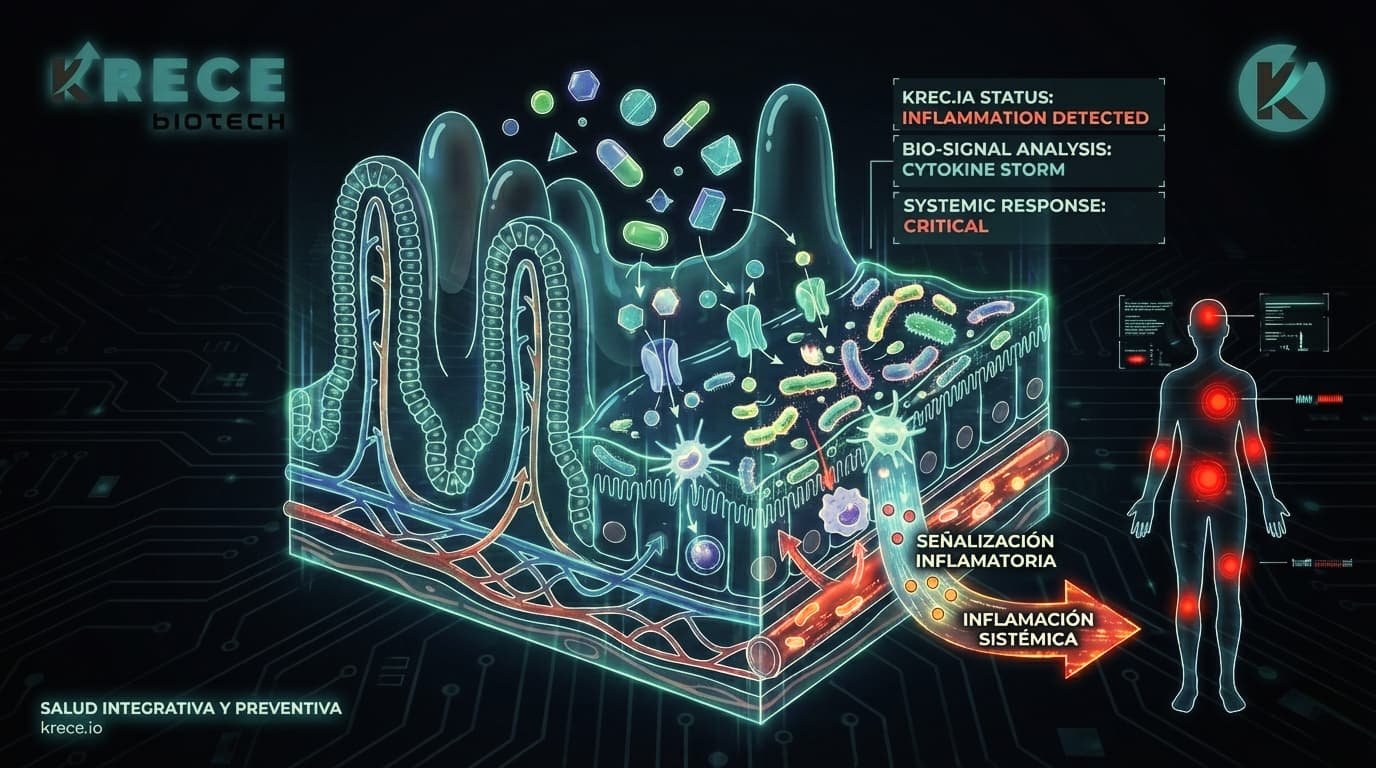
Barrera intestinal y translocación inflamatoria
El mecanismo fisiopatológico que conecta la disbiosis con la inflamación sistémica es la pérdida de la integridad de la barrera intestinal. El epitelio intestinal actúa como una interfaz selectiva que debe permitir el paso de nutrientes mientras bloquea la entrada de antígenos y toxinas microbianas.
Cuando las uniones estrechas (tight junctions) se debilitan debido a factores estresores o disbióticos, aumenta la permeabilidad paracelular. Esto permite la translocación de patrones moleculares asociados a patógenos (PAMPs) desde el lumen hacia la lámina propia y la circulación portal. El agente más relevante en este proceso es el lipopolisacárido (LPS), un componente de la membrana externa de las bacterias Gram-negativas.
La presencia de LPS en sangre, conocida como endotoxemia metabólica, activa los receptores Toll-like 4 (TLR4) en macrófagos y otras células inmunitarias, desencadenando la cascada del factor nuclear kappa B (NF-$\kappa$B) y la liberación masiva de citoquinas proinflamatorias como IL-6, TNF-$\alpha$ e IL-1$\beta$.
Metabolitos microbianos y señalización inmune
La modulación de la inflamación no depende únicamente de evitar la translocación de endotoxinas, sino también de la presencia de señales activas de resolución. En este contexto, los metabolitos derivados de la fermentación bacteriana de la fibra, específicamente los ácidos grasos de cadena corta (AGCC) como el butirato, el propionato y el acetato, juegan un rol crítico.
Los AGCC actúan como ligandos para receptores acoplados a proteínas G (GPR43, GPR109A) en la superficie de las células inmunitarias y epiteliales, ejerciendo potentes efectos antiinflamatorios. Mecanísticamente, el butirato inhibe las histonas desacetilasas (HDAC), lo que resulta en una regulación epigenética que suprime la expresión de genes proinflamatorios y potencia la diferenciación de células Treg. La ausencia de estos metabolitos debido a una microbiota empobrecida elimina este freno fisiológico, exacerbando la respuesta inflamatoria sistémica.
Inflammaging como consecuencia sistémica
El inflammaging se define como la cronificación de esta respuesta inmune innata. La exposición continua a la endotoxemia metabólica y la falta de señalización reguladora por AGCC conducen a un agotamiento del sistema inmune y a una acumulación de células senescentes.
Estas células senescentes adquieren un fenotipo secretor asociado a la senescencia (SASP), liberando continuamente citoquinas proinflamatorias, quimiocinas y proteasas que degradan la matriz extracelular y afectan a las células vecinas sanas. Este círculo vicioso de inflamación y daño tisular no localizado afecta a órganos distantes, promoviendo la resistencia a la insulina, la disfunción endotelial y la neuroinflamación. El intestino, por tanto, actúa como el motor que perpetúa el fuego inflamatorio del envejecimiento.
Impacto en longevidad funcional
La longevidad funcional depende de la capacidad del organismo para mantener la flexibilidad metabólica y la reparación celular. La inflamación sistémica derivada de la disbiosis compromete estos procesos al desviar recursos energéticos hacia la respuesta inmune y aumentar el estrés oxidativo mitocondrial.
La integridad de la red immuno-metabólica es el determinante final de la velocidad de envejecimiento. Una microbiota resiliente y una barrera intacta previenen la sobreactivación del sistema inmune innato, reduciendo la carga alostática y preservando la funcionalidad de los tejidos. Entender la modulación microbiana de la inflamación es, en última instancia, entender la biología molecular del envejecimiento saludable.
Conclusión: El intestino como marcapasos del envejecimiento
La integración de la evidencia fisiológica obliga a reevaluar la naturaleza del envejecimiento. Lejos de ser un deterioro pasivo dictado exclusivamente por el calendario, la senescencia biológica se revela como un proceso activo de desgaste inmunometabólico, donde el intestino ejerce de rector central. El fenómeno del inflammaging demuestra que la velocidad a la que envejece un organismo es directamente proporcional a su carga inflamatoria sistémica.
La transición desde la salud funcional hacia la fragilidad se precipita cuando se rompe la alianza simbiótica. La permeabilidad de la barrera y la pérdida de metabolitos reguladores transforman al intestino de un aliado metabólico en una fuente crónica de endotoxemia y estrés oxidativo. En última instancia, modular la señalización microbiana no constituye una estrategia para mejorar la digestión, sino el mecanismo fundamental para desacelerar el reloj biológico, preservar la flexibilidad metabólica y mantener la competencia sistémica frente al paso del tiempo.
Responsabilidad Editorial
Este contenido forma parte del proyecto editorial KRECE, una plataforma independiente dedicada al análisis, síntesis y divulgación de evidencia científica en salud, longevidad y biología humana.
Los artículos publicados en KRECE se elaboran a partir de literatura científica revisada (revisiones sistemáticas, meta-análisis y ensayos clínicos), utilizando metodologías de evaluación estructurada como el marco PICO (Población, Intervención, Comparación y Resultados).
El contenido se elabora utilizando herramientas de apoyo para el análisis y síntesis de información, bajo un modelo de supervisión humana constante. La interpretación biológica, la validación de fuentes y la decisión final de publicación corresponden siempre al equipo editorial de KRECE.
Puedes conocer en detalle nuestra metodología y principios editoriales en:
- Microbiota e inflamación basal
- Barrera intestinal y endotoxemia metabólica
- AGCC y señalización inmune
- Inflammaging como proceso sistémico
- Impacto en longevidad funcional