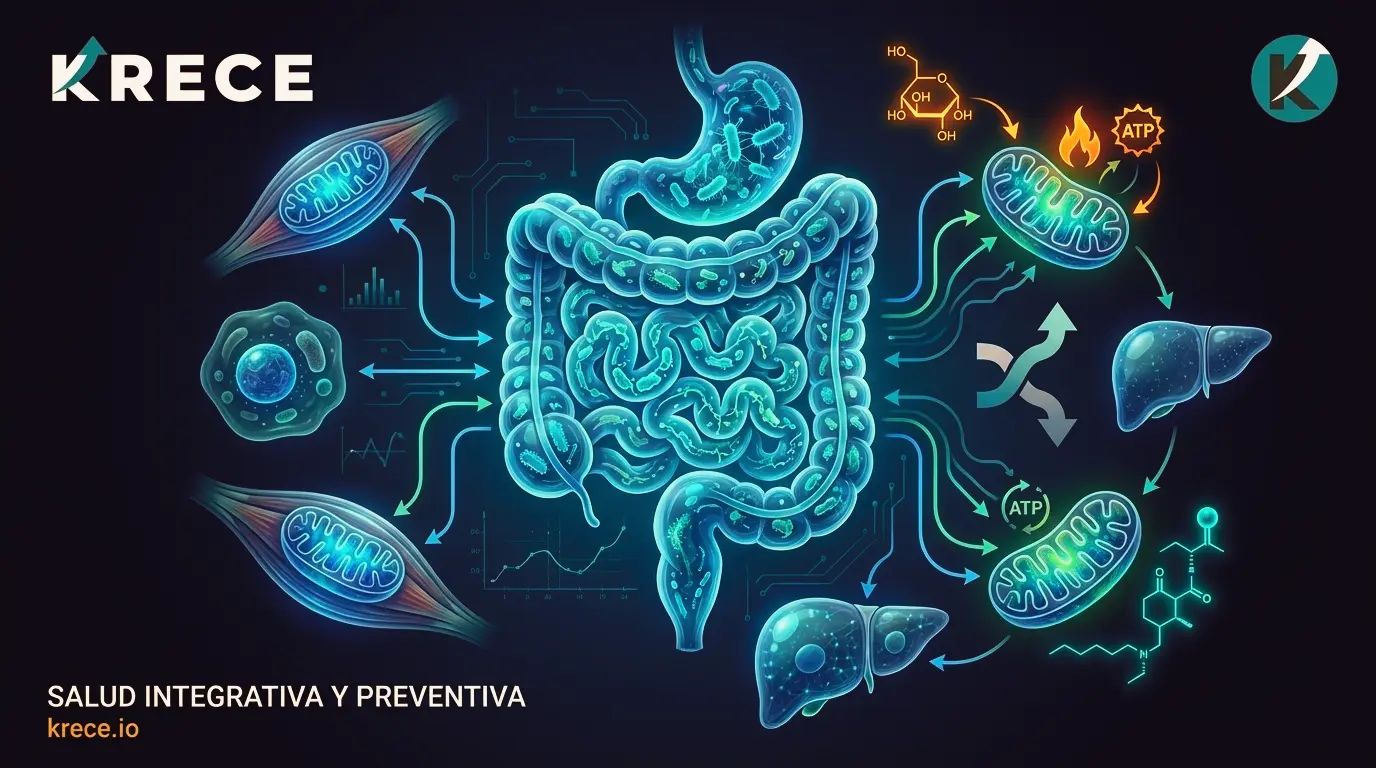
La flexibilidad metabólica se define fisiológicamente como la capacidad celular para alternar eficientemente entre la oxidación de glucosa y la oxidación de lípidos en función de la disponibilidad de sustratos y la demanda energética. Aunque la ejecución de este cambio de combustible ocurre en las mitocondrias de tejidos periféricos, la señalización que autoriza o bloquea dicho proceso está fuertemente condicionada por la actividad de la microbiota como órgano metabólico.
El ecosistema intestinal no se limita a procesar nutrientes; actúa como un regulador upstream de los sensores energéticos celulares, modulando la plasticidad metabólica a través de dos vías principales: la señalización por metabolitos y la regulación del tono inflamatorio sistémico.
Señalización mediada por metabolitos y sensores energéticos
La microbiota influye en la selección del sustrato energético mediante la producción de moléculas señalizadoras que ingresan a la circulación portal. Entre estas, los ácidos grasos de cadena corta (AGCC)ejercen una función pleiotrópica sobre la maquinaria oxidativa del huésped.
Mecanísticamente, moléculas como el butirato y el propionato actúan como ligandos de receptores acoplados a proteínas G (GPR41, GPR43) y, fundamentalmente, como moduladores de la actividad de la AMPK (proteína quinasa activada por AMP). La fosforilación de AMPK es el evento molecular crítico que inhibe la síntesis de ácidos grasos y activa la beta-oxidación mitocondrial (CPT-1). Asimismo, estos metabolitos bacterianos influyen en la acetilación de histonas, facilitando la transcripción de PGC-1α, el coactivador maestro de la biogénesis mitocondrial. Sin esta señalización basal derivada de la fermentación intestinal, la capacidad de la célula para adaptar su maquinaria enzimática a la oxidación de grasas se ve comprometida.
Inflamación de bajo grado y bloqueo de la oxidación lipídica
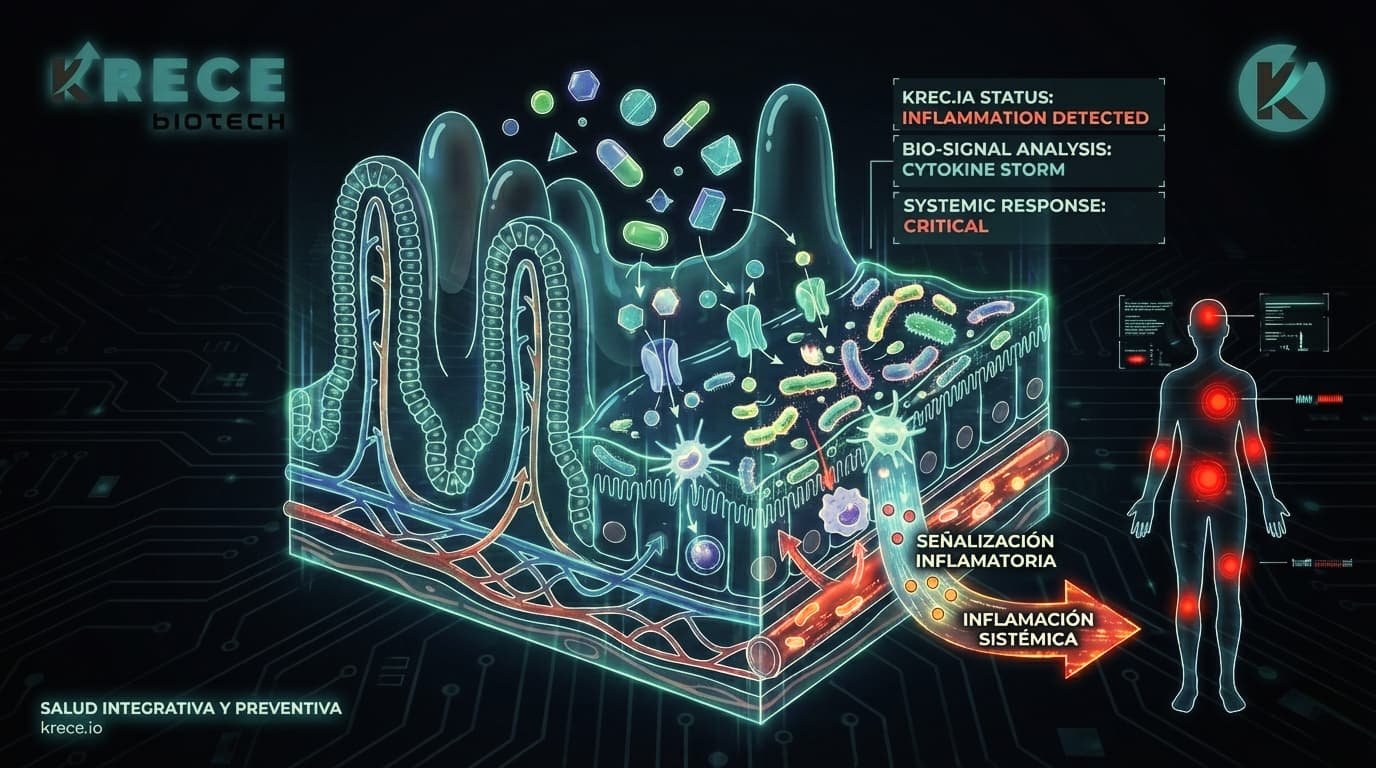
La pérdida de flexibilidad metabólica, caracterizada por una dependencia continua de la glucosa y una incapacidad para oxidar lípidos en estado de ayuno, correlaciona directamente con la permeabilidad del epitelio intestinal. Cuando la integridad de la barrera intestinal se ve vulnerada, la translocación de lipopolisacáridos (LPS) al torrente sanguíneo induce una respuesta inmunitaria subclínica.
La activación de receptores TLR4 por endotoxinas interfiere con la señalización de la insulina mediante la fosforilación inhibitoria del sustrato IRS-1 en residuos de serina/treonina. En este contexto inflamatorio, el metabolismo celular se reprograma hacia una glucólisis prioritaria —en una dinámica análoga a un efecto Warburg—, bloqueando la entrada de ácidos grasos a la mitocondria para preservar recursos ante la señal de alarma inmunológica. Este estado de «rigidez metabólica» es, por tanto, una respuesta adaptativa a una señalización proinflamatoria originada en el intestino.
El eje microbiota-mitocondria como regulador sistémico
La comunicación entre microbiota y mitocondrias es bidireccional y evolutivamente conservada. Los metabolitos bacterianos no solo sirven de sustrato, sino que modulan la eficiencia de la cadena de transporte de electrones y la producción de especies reactivas de oxígeno (ROS). Una microbiota en eubiosis mantiene un tono de señalización que optimiza la fosforilación oxidativa, permitiendo que la mitocondria responda ágilmente a los cambios de sustrato.
Por el contrario, la disrupción de esta comunicación genera un desacoplamiento funcional que impide la correcta alternancia de combustibles. Este mecanismo subraya que la flexibilidad metabólica y longevidad funcional están supeditadas a la homeostasis de este eje, donde el intestino dicta la capacidad del organismo para gestionar sus reservas energéticas.
📐 Ver esquema editorial KRECE
Tipo de contenido: Cluster
Silo: /microbiota/
Rol editorial: Mecanismo fisiológico dependiente
Función: Explicar cómo la microbiota modula la flexibilidad metabólica mediante señalización metabólica, inflamación y función mitocondrial.