La retirada de agonistas GLP-1 desencadena una serie de adaptaciones neuroendocrinas que afectan a la señalización de saciedad y a la homeostasis energética sistémica.
La administración exógena de análogos del péptido similar al glucagón tipo 1 (GLP-1) induce una modificación en la regulación homeostática del peso corporal, actuando sobre los núcleos hipotalámicos encargados del control del apetito. La interrupción de estos estímulos farmacológicos desencadena una respuesta fisiológica compensatoria caracterizada por una recuperación ponderal. Este fenómeno responde a una recalibración del set point energético, mediada por la plasticidad neuronal y la memoria metabólica del tejido adiposo.
El proceso implica la interacción entre la desensibilización de receptores periféricos y centrales, la alteración en la sensibilidad a la insulina y homeostasis energética, y la respuesta inflamatoria sistémica derivada de la fluctuación de la masa grasa.
MECANISMOS DE DESREGULACIÓN NEUROENDOCRINA POST-INTERVENCIÓN
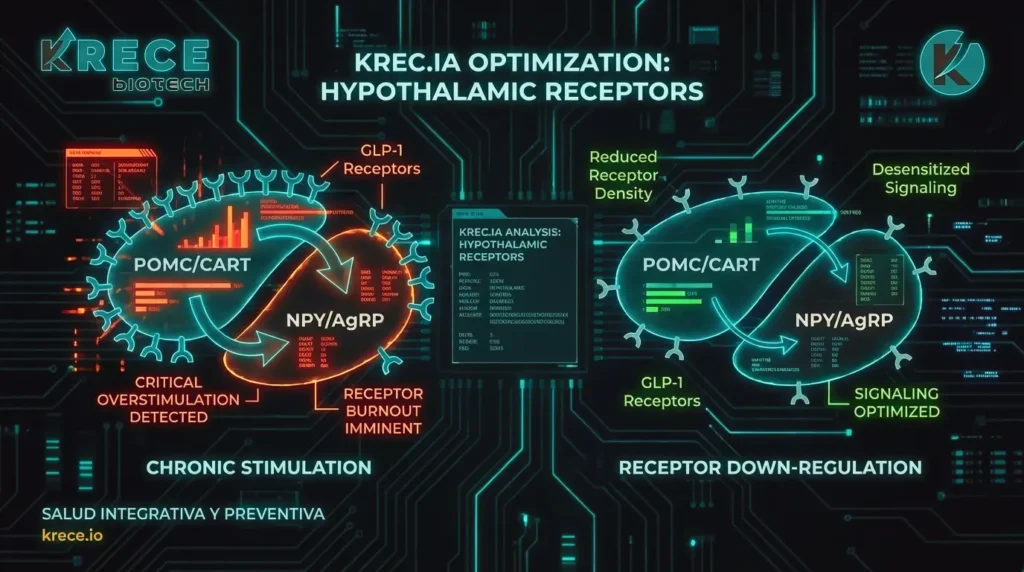
El mecanismo de acción de los agonistas de GLP-1 se basa en la estimulación de las neuronas POMC/CART (anorexigénicas) y la inhibición de las neuronas NPY/AgRP (orexigénicas) en el núcleo arqueado del hipotálamo. Durante la exposición continua, se produce una adaptación funcional de los receptores GLP-1R debido a la presencia crónica del ligando.
Adaptación hipotalámica y señalización orexigénica post-retirada
Al retirar el estímulo exógeno, la producción endógena de GLP-1 —secretada por las células L del ileon en respuesta a la ingesta— interactúa con receptores cuya densidad o sensibilidad ha disminuido (down-regulation). Esto resulta en un rebote en la señalización orexigénica, donde la inhibición sobre el NPY (neuropéptido Y) desaparece, generando una señal de apetito superior a las necesidades energéticas basales.
LA DEUDA ENERGÉTICA Y LA MEMORIA DEL ADIPOCITO
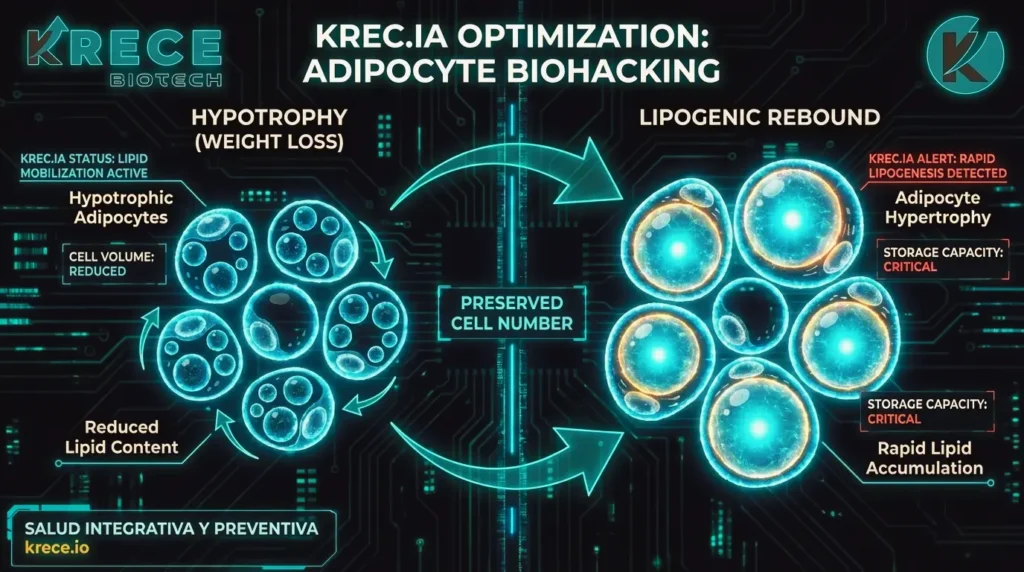
El tejido adiposo blanco actúa como un órgano endocrino dinámico. Durante la pérdida de peso inducida farmacológicamente, se observa una reducción en el volumen de los adipocitos (hipotrofia), manteniéndose su número (hiperplasia remanente). Al cesar la intervención, estos adipocitos presentan un estado de avidez lipogénica.
Esta respuesta se asocia al «gap hormonal» post-tratamiento:
- Hipo-leptinemia relativa: Los niveles de leptina descienden en proporción a la reducción de masa grasa, señalizando al sistema nervioso central un estado de déficit energético.
- Hiper-grelinemia reactiva: La grelina gástrica aumenta como mecanismo compensatorio.
Esta configuración hormonal dificulta la flexibilidad metabólica, favoreciendo el almacenamiento de sustratos y la recuperación de la masa grasa para restaurar el set point previo.
IMPACTO EN LA COMPOSICIÓN CORPORAL Y RIESGO INFLAMATORIO
La pérdida de peso acelerada mediante agonistas GLP-1 puede conllevar una reducción de tejido magro (músculo esquelético). Si tras la retirada del fármaco la recuperación de peso se produce predominantemente en forma de masa grasa, el fenotipo resultante presenta una composición corporal alterada.
La fluctuación ponderal rápida y la expansión del tejido adiposo visceral se asocian a una elevación de marcadores de estrés oxidativo y citoquinas (IL-6, TNF-α). Este estado de weight cycling actúa como inductor de inflammaging, afectando a la resistencia a la insulina basal.
ANÁLISIS DE EVIDENCIA: RETIRADA DE AGONISTAS Y DINÁMICA PONDERAL
SÍNTESIS FISIOPATOLÓGICA: RECAPITULACIÓN MECANÍSTICA
El análisis de la respuesta biológica tras la supresión de agonistas GLP-1 describe una secuencia de eventos homeostáticos compensatorios:
- Down-regulation de receptores: La exposición prolongada a ligandos exógenos reduce la densidad o sensibilidad de los receptores GLP-1R, limitando la eficacia de la señalización endógena post-retirada.
- Inercia Lipogénica: El tejido adiposo mantiene una capacidad de almacenamiento preservada, que se activa ante el balance energético positivo resultante de la desinhibición del apetito.
- Desacople de la señalización de saciedad: La discordancia entre la masa grasa reducida y los niveles circulantes de leptina y grelina impulsa la ingesta calórica hasta restablecer el equilibrio energético previo a la intervención.
Responsabilidad editorial
📚 Ver Referencias Científicas y Estudios
- Weight regain and cardiometabolic effects after withdrawal of semaglutide: The STEP 1 trial extension – (2022)
- GLP-1 receptor agonist withdrawal and subsequent weight regain: A systematic review – (2024)
- Physiological mechanisms of weight regain following pharmacotherapy cessation – (2026)
📐 Ver esquema editorial KRECE
- Silo: Hormonas
- Tipo: Cluster mecanístico aplicado
- Dependencias: Sensibilidad a la insulina · Flexibilidad metabólica · Inflammaging
- Rol: Describir la desregulación de la señalización de saciedad tras retirada de estímulos hormonales exógenos
Conclusiones y Cierre
La evidencia analizada permite establecer que la recuperación ponderal tras el cese de agonistas del receptor GLP-1 no constituye un fallo conductual, sino una respuesta fisiológica predecible y multifactorial. La intervención farmacológica, si bien eficaz para la supresión temporal de la señalización orexigénica, no modifica la arquitectura base de la homeostasis energética a largo plazo si no se acompaña de una reestructuración metabólica profunda.
La fisiopatología del rebote se articula sobre tres ejes mecanísticos que perpetúan la obesidad como condición crónica recurrente:
- Hipersensibilidad orexigénica: La down-regulation de receptores inducida por dosis suprafisiológicas genera una respuesta de hambre exacerbada ante la caída de los niveles del fármaco.
- Disociación lipo-hormonal: La asincronía entre la masa grasa reducida y los niveles circulantes de leptina impide la correcta señalización de suficiencia energética al hipotálamo.
- Inflexibilidad metabólica: La persistencia de una maquinaria celular optimizada para el almacenamiento lipídico (lipogénesis de novo) frente a la oxidación de sustratos.
KRECE: PERSPECTIVA LONGEVIDAD
La estabilidad en la señalización neuroendocrina es un componente fundamental de la homeostasis sistémica a lo largo del tiempo. Las fluctuaciones cíclicas de peso inducen adaptaciones celulares y estrés oxidativo que afectan a la función metabólica basal y a la preservación de la masa magra, elementos centrales en la biología del envejecimiento.
Desde una perspectiva de biología fundamental, la estrategia de manejo de peso a largo plazo requiere trascender la simple restricción calórica o la supresión química del apetito. El foco debe desplazarse hacia la restauración de la sensibilidad a la insulina, la preservación de la masa magra como tejido endocrino activo y la modulación de los circuitos de recompensa mediante la densidad nutricional, elementos indispensables para evitar la cronificación del ciclo de pérdida y recuperación de peso (weight cycling) y sus consecuencias inflamatorias sistémicas.



