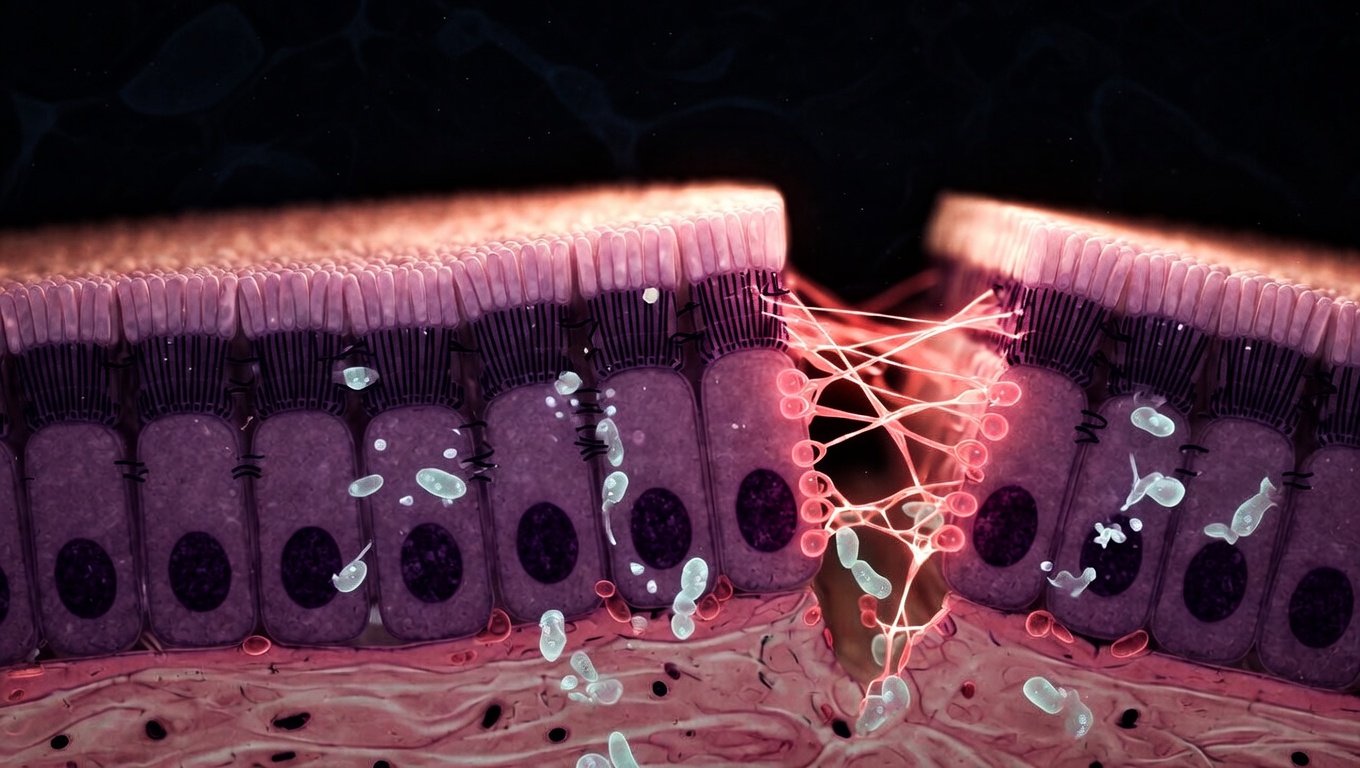
Barrera Intestinal, Permeabilidad y Disbiosis
Si llevas meses — o años — con hinchazón después de cada comida, intolerancias alimentarias que se multiplican, fatiga que no se explica con un análisis de sangre normal, o una enfermedad autoinmune que nadie conecta con tu intestino, este protocolo está escrito para ti. Vamos a identificar qué está fallando, qué tiene evidencia para repararlo, y qué es ruido.
La permeabilidad intestinal no aparece en una radiografía ni se diagnostica con un análisis de rutina. Se manifiesta como un patrón de síntomas que la medicina convencional suele tratar por separado sin conectarlos. Si reconoces tres o más de estos signos de forma crónica (no puntual), tu barrera intestinal merece una evaluación específica.
La gastroenterología convencional no reconoce el «intestino permeable» como diagnóstico primario. El término científico aceptado es hiperpermeabilidad intestinal, y se considera un hallazgo fisiopatológico, no una enfermedad en sí misma. El test más fiable es el de lactulosa-manitol (funcional, mide permeabilidad in vivo). La zonulina fecal y los anticuerpos anti-LPS son complementarios. Lleva esta información a tu médico — no todos conocen estas pruebas.
Tu intestino tiene el grosor de una sola célula. Esa capa separa todo lo que comes del torrente sanguíneo donde reside el 70% de tu sistema inmune. Las células están unidas entre sí por unas proteínas llamadas uniones estrechas (tight junctions) que actúan como «cremalleras» entre ellas. Cuando estas cremalleras se abren, fragmentos de bacterias, toxinas y proteínas alimentarias se filtran a la sangre. Tu sistema inmune los detecta, entra en modo de ataque permanente, y el resultado es inflamación crónica sistémica.
Tres vectores explican por qué ocurre:
Vector 1: Zonulina y apertura de las uniones estrechas
La zonulina es una proteína producida por tu propio intestino que regula la apertura y cierre de las tight junctions. En condiciones normales, las abre transitoriamente para dejar pasar nutrientes. En la permeabilidad patológica, la zonulina está sobreexpresada — las cremalleras se quedan abiertas permanentemente. El disparador más documentado: la gliadina (proteína del gluten), que se une al receptor CXCR3 del enterocito y fuerza la liberación de zonulina incluso en personas no celíacas.
La gliadina se une al receptor de quimioquinas CXCR3 en la superficie apical de los enterocitos. Esto desencadena la liberación de zonulina al espacio intercelular. La zonulina interacciona con los complejos proteicos de las tight junctions (claudinas, ocludina, ZO-1), provocando su desacoplamiento. El resultado es una apertura paracelular que permite la translocación de macromoléculas, antígenos alimentarios y lipopolisacáridos (LPS) bacterianos al espacio subepitelial, donde son captados por las células dendríticas y presentados al sistema inmune adaptativo. Este mecanismo fue descrito por el Dr. Alessio Fasano (Harvard/MGH) y es la base fisiopatológica de la enfermedad celíaca y la sensibilidad al gluten no celíaca.
Vector 2: Endotoxemia metabólica (LPS)
Cuando la barrera se abre, los lipopolisacáridos (LPS) — toxinas de la membrana de las bacterias intestinales — pasan a la sangre. Tu hígado y sistema inmune detectan estas endotoxinas y lanzan una cascada inflamatoria permanente. Esto se llama endotoxemia metabólica: una intoxicación crónica de bajo grado que inflama tejidos a distancia — articulaciones, cerebro, tiroides, piel. Es el puente entre tu intestino y prácticamente cualquier enfermedad crónica.
Vector 3: Disbiosis y pérdida del escudo bacteriano
Tu microbiota intestinal produce ácidos grasos de cadena corta (especialmente butirato) que alimentan las células del colon y mantienen la integridad de la barrera. Cuando la diversidad bacteriana colapsa — por antibióticos, dieta ultraprocesada, estrés crónico o AINEs — la producción de butirato cae, la capa de moco protectora se degrada, y las tight junctions pierden su soporte. La disbiosis no es solo un desequilibrio de bacterias: es la caída del sistema de mantenimiento de tu barrera.
La permeabilidad intestinal está documentada como factor contribuyente o «puerta de entrada» en múltiples condiciones autoinmunes. En diabetes tipo 1, la hiperpermeabilidad mediada por zonulina precede clínicamente al debut de la enfermedad: antígenos cruzan la barrera y provocan mimetismo molecular contra células beta pancreáticas. En Hashimoto, la gliadina cruza la barrera y genera autoanticuerpos (anti-TPO, anti-TG) contra tejido tiroideo por similitud estructural con la proteína del gluten. En esclerosis múltiple, existe correlación entre permeabilidad intestinal y permeabilidad de la barrera hematoencefálica. En artritis reumatoide, la proliferación de bacterias gramnegativas (Prevotella, Klebsiella) genera una respuesta Th17 que ataca el tejido sinovial. En vitíligo, la disbiosis intestinal y la inflamación sistémica contribuyen a la destrucción de melanocitos.
El mercado de la salud intestinal es un campo minado de marketing disfrazado de ciencia. Esto es lo que dice la evidencia clínica real, no los influencers.
Reparar la barrera intestinal no es comprar un suplemento. Es una secuencia de intervenciones en el orden correcto: primero eliminar lo que destruye, luego reparar, luego reinocular y mantener. Cualquier suplemento que prometa revertir la permeabilidad sin exigir cambios en lo que comes, bebes y tomas está en el terreno del marketing, no de la biología.
Fase 1: Eliminar (semanas 1–4)
No puedes reparar una pared mientras alguien sigue golpeándola. Antes de cualquier suplemento, retira lo que está dañando la barrera.
AINEs y fármacos gastrotóxicos. Ibuprofeno, naproxeno, aspirina crónica — bloquean COX-1, inhiben prostaglandinas protectoras y destruyen la mucosa directamente. Si los necesitas por dolor crónico, busca alternativas con tu médico. Los inhibidores de bomba de protones (omeprazol) usados crónicamente también alteran el pH gástrico y promueven disbiosis.
Eliminación temporal de gluten. 4–8 semanas sin gluten estricto. No por moda — por la vía documentada gliadina → zonulina → apertura de tight junctions. Si los síntomas mejoran significativamente, tienes tu respuesta. Si no mejoran, reintroduce y descarta otros disparadores.
Alcohol, ultraprocesados y azúcar refinado. El alcohol aumenta directamente la permeabilidad intestinal. Los ultraprocesados carecen de fibra prebiótica y contienen emulsificantes (polisorbato-80, carboximetilcelulosa) que degradan la capa de moco protectora.
Descartar SIBO y H. pylori. Si hay hinchazón excesiva, gases y eructos crónicos, descartar sobrecrecimiento bacteriano con test de aliento (hidrógeno/metano). El H. pylori se descarta con antígeno fecal. Tratar antes de reparar — no tiene sentido sellar un intestino con infección activa.
Fase 2: Reparar (semanas 2–12)
Se solapa con la Fase 1. Una vez que los agresores están eliminados o reducidos, introducimos las herramientas de reparación.
| Compuesto | Dosis | Función |
|---|---|---|
| Zinc Carnosina | 75 mg 2x/día | Reparación directa de tight junctions. Primera línea. El compuesto con más evidencia específica para permeabilidad. |
| Butirato / Tributirina | 300–600 mg 2x/día | Combustible del colonocito. Efecto epigenético antiinflamatorio. Tributirina es la forma oral más biodisponible. |
| L-Glutamina | 5–10 g/día (subir a 20–25 g si tolera) | Substrato energético del enterocito. Empezar con dosis baja y subir. No dar si hay disbiosis severa sin tratar. |
| S. boulardii | 500 mg 1–2x/día | Protector antipatogénico. No coloniza — actúa transitóriamente. Especialmente útil post-antibióticos. |
| L. rhamnosus GG | 10–20 mil millones UFC | Estabilizador de barrera. Reducción de citoquinas proinflamatorias. Usar cepa GG verificada, no genérico. |
| Vitamina D3 + K2 | 5.000 UI/día (ajustar por analítica) | Inmunomodulador. Estimula linfocitos T reguladores (T-reg) que frenan la cascada autoinmune Th17. |
Capa peptídica (donde el marco regulatorio lo permita): BPC-157 oral (250–500 mcg, estómago vacío) + KPV oral (500 mcg). El BPC-157 repara la estructura (angiogénesis, tight junctions). El KPV apaga la inflamación (NF-κB). La sinergia es lógica biológicamente pero no está demostrada en ECA. Esta capa es N1 — decírselo al paciente con honestidad total.
BPC-157 está en FDA Categoría 2 desde septiembre 2023 (prohibido en compounding en EE.UU.). En mercados LATAM (Paraguay, Argentina, Colombia) y Europa, el marco regulatorio es diferente. KRECE no comercializa BPC-157 bajo la marca SIGNALS. El PDA (Pentadeca Arginato) se clasifica como N0 — cero estudios independientes publicados. No extrapolar.
Fase 3: Reinocular y mantener
La reparación sin mantenimiento es temporal. La barrera necesita alimentación continua.
Fibra prebiótica diversa. Mínimo 30 fuentes vegetales diferentes por semana (no 30 raciones — 30 tipos). Incluir inulina, FOS, almidón resistente (plátano verde, arroz enfriado), pectina (manzana). La diversidad alimenta las bacterias productoras de butirato (Faecalibacterium prausnitzii, Akkermansia muciniphila).
Alimentos fermentados. Chucrut, kimchi, kefir, kombucha — no como suplemento sino como hábito diario. La evidencia muestra que los alimentos fermentados aumentan la diversidad bacteriana más que la fibra sola (estudio Stanford, Cell 2021).
Reintroducción controlada. Después de 4–8 semanas de eliminación, reintroducir un alimento cada 3–4 días. Observar síntomas durante 72 horas. Si hay reacción, retirar y reevaluar en 3 meses. El objetivo no es evitar alimentos de por vida — es identificar disparadores y restaurar tolerancia.
Señales de que funciona: reducción de la hinchazón post-prandial, deposiciones más formadas y regulares, tolerancia alimentaria que se amplía, energía post-comida en lugar de fatiga, mejora de marcadores inflamatorios (PCR, calprotectina fecal) y autoinmunes (anti-TPO si aplica).
La reparación de la barrera intestinal es el protocolo más infravalorado de la medicina moderna. Y el más contaminado por el marketing de suplementos.
La ciencia de la permeabilidad intestinal es real. El descubrimiento de la zonulina por Fasano, la documentación de la endotoxemia metabólica, y la conexión con la autoinmunidad son mecanismos validados con rigor. Lo que no es real es la mayoría de las soluciones que se venden para tratarla.
La primera línea no es un péptido, ni un suplemento exotíco, ni un test de microbioma de 300 dólares. Es aburridamente efectiva: eliminar AINEs, retirar gluten durante 4–8 semanas para evaluar, añadir zinc carnosina (75 mg 2x/día) y butirato (tributirina), e incorporar S. boulardii y L. rhamnosus GG como únicos probióticos con datos reales. Eso cubre N4–N5 de evidencia y no cuesta una fortuna.
El BPC-157 oral es, en nuestra opinión, el compuesto preclínico más fascinante de la gastroenterología regenerativa. Los 500+ estudios sobre reparación de mucosa, tight junctions y daño por AINEs son impresionantes. Pero tenemos que ser honestos: cero ECA publicados en humanos, 80% de la investigación de un solo laboratorio, ensayos Fase 2 cuyos resultados nunca se publicaron. Eso no es N4. Es N1 con un asterisco enorme. En KRECE lo mantenemos fuera del catálogo SIGNALS por su estatus FDA Categoría 2, pero reconocemos su valor en jurisdicciones donde el compounding magistral sigue siendo legal.
El KPV oral tiene una lógica biológica elegante — absorción intestinal vía PepT1 y silenciamiento de NF-κB. Pero comparte la misma limitación: N1 sin datos humanos controlados.
Si este fuera mi protocolo personal: eliminación de disparadores (semanas 1–2), zinc carnosina + tributirina como base (semana 1 en adelante), ayuno intermitente 16:8, fibra prebiótica diversa, S. boulardii durante y después de cualquier antibiótico, y vitamina D en rango 60–80 ng/mL. Si después de 8 semanas los síntomas persisten, añadiría BPC-157 oral (donde sea legal y con fuente verificada por CoA independiente). El KPV como capa adicional si la inflamación no cede con lo anterior.
Lo que descartamos: caldo de huesos como terapia, limpiezas de colon, probióticos genéricos sin cepa identificada, tests de microbioma directos al consumidor como base para prescripción, y cualquier promesa de «reparar el intestino en 30 días» sin cambio de hábitos. Si no te piden que cambies lo que comes, te están vendiendo algo.